2011년04월12일 10번
[과목 구분 없음] 그림은 일정량의 묽은 염산(HCl)에 수산화나트륨(NaOH) 수용액의 부피를 달리하여 혼합하였을 때, 발생하는 열량을 상대값으로 나타낸 것이다.
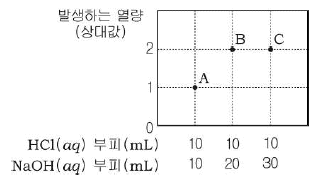
혼합 용액 A~C에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, HCl(aq), NaOH(aq)의 처음 온도는 같다.) [3점]

혼합 용액 A~C에 대한 설명으로 옳은 것만을 <보기>에서 있는 대로 고른 것은? (단, HCl(aq), NaOH(aq)의 처음 온도는 같다.) [3점]

- ① ㄱ
- ② ㄷ
- ③ ㄱ, ㄴ
- ④ ㄴ, ㄷ
- ⑤ ㄱ, ㄴ, ㄷ
(정답률: 알수없음)
문제 해설
보기에서 "ㄱ"은 혼합 용액의 온도가 모두 상승하는 것을 나타내고, "ㄴ"은 혼합 용액의 온도가 모두 하락하는 것을 나타낸다. 이는 열량이 발생하는 반응이 일어나기 때문인데, HCl과 NaOH가 반응하여 열이 발생하면서 혼합 용액의 온도가 변화하는 것이다. 따라서, HCl과 NaOH의 양이 일정하게 증가하면서 혼합 용액의 온도가 일정하게 상승하는 경우에는 "ㄱ"이 옳고, HCl과 NaOH의 양이 일정하게 증가하면서 혼합 용액의 온도가 일정하게 하락하는 경우에는 "ㄴ"이 옳다. 그러나, 혼합 용액의 온도가 먼저 상승하다가 어느 순간부터 하락하는 경우에는 "ㄱ, ㄴ"이 모두 옳다. 이는 HCl과 NaOH의 양이 일정하게 증가하다가 어느 순간부터는 반응이 포화되어 열이 발생하지 않고 오히려 흡열반응이 일어나서 온도가 하락하기 때문이다. 따라서, "ㄱ, ㄴ"이 정답이다.
연도별
- 2016년09월01일
- 2016년07월06일
- 2016년06월02일
- 2016년04월06일
- 2016년03월10일
- 2015년11월12일
- 2015년10월13일
- 2015년09월02일
- 2015년07월09일
- 2015년06월04일
- 2015년04월09일
- 2015년03월11일
- 2014년11월13일
- 2014년10월07일
- 2014년09월03일
- 2014년07월10일
- 2014년06월12일
- 2014년04월10일
- 2014년03월12일
- 2013년11월07일
- 2013년10월08일
- 2013년09월03일
- 2013년07월12일
- 2013년06월05일
- 2013년04월11일
- 2013년03월13일
- 2012년11월08일
- 2012년10월09일
- 2012년09월04일
- 2012년07월11일
- 2012년06월07일
- 2012년04월10일
- 2011년10월12일
- 2011년09월01일
- 2011년07월13일
- 2011년06월02일
- 2011년04월12일
- 2011년02월28일
- 2010년11월18일
- 2010년10월12일
- 2010년09월02일
- 2010년07월08일
- 2010년06월10일
- 2010년04월13일
- 2010년03월12일
- 2009년11월12일
- 2009년10월15일
- 2009년09월03일
- 2009년07월14일
- 2009년06월04일
- 2009년04월15일
- 2009년03월13일
- 2008년11월13일
- 2008년10월16일
- 2008년09월04일
- 2008년07월15일
- 2008년06월04일
- 2008년04월15일
- 2008년03월14일
- 2007년11월15일
- 2007년10월10일
- 2007년09월06일
- 2007년07월12일
- 2007년06월07일
- 2007년03월16일
- 2006년11월16일
- 2006년10월12일
- 2006년09월06일
- 2006년06월03일
- 2006년04월19일
- 2006년03월11일

